Hvad bruger man elektrolyse til, og hvad er det?
I bestræbelserne på at finde bæredygtige energiløsninger er brint blevet en central spiller på grund af dets potentiale til at levere ren energi uden udledning af drivhusgasser. En vigtig del af denne grønne revolution er elektrolyseanlægget, en enhed der spalter vand til brint og ilt ved hjælp af elektricitet. Men hvordan kan elektrolyse bruges til at producere brint? Lad os dykke ned i processen, elektrolyse af vand effektivitet, og de forskellige metoder, der bruges til at producere brint gennem elektrolyse.
Et elektrolyseanlæg er en enhed, der bruger elektricitet til at spalte vand (H₂O) i brint (H₂) og ilt (O₂). Hvad er elektrolyse? Denne proces, kendt som elektrolyse, indebærer, at en elektrisk strøm ledes gennem vand, hvilket udløser en kemisk reaktion, der adskiller molekylerne i deres bestanddele. Hvordan kan elektrolyse bruges til at producere brint? Elektrolyse til produktion af brint er en lovende metode til at generere brændstof, især når det drives af vedvarende energikilder som vind- eller solenergi. Se den følgende illustration:
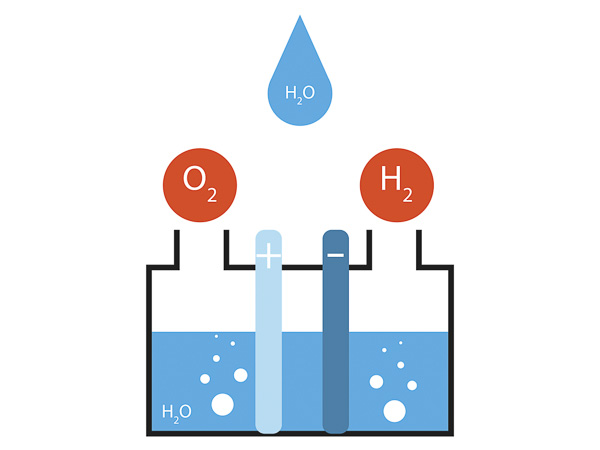
To elektroder i vand - en positiv og en negativ - frigiver gasserne under reaktionen.
Hvordan fungerer et brint elektrolyseanlæg?
Elektrolyse er en proces, der involverer en elektrolytisk celle, bestående af to elektroder (en anode og en katode) og en elektrolyt. Når en jævnstrøm påføres, oxideres vandmolekyler ved anoden og producerer iltgas og positivt ladede brintioner (protoner). Disse protoner bevæger sig gennem elektrolytten til katoden, hvor de kombineres med elektroner og danner brintgas. Hvor effektiv er elektrolyse? Dette kan repræsenteres ved følgende reaktioner:
- Anode reaktion: 2H₂O → O₂ + 4H⁺ + 4e⁻
- Katode reaktion: 4H⁺ + 4e⁻ → 2H₂
Ren vedvarende energi og produktion af grøn brint
Brintens sande potentiale som en ren energikilde realiseres, når ren vedvarende energi, som sol, vind eller vandkraft, bruges til at drive elektrolyseprocessen. Denne metode producerer det, der er kendt som grøn brint, som er helt kulstoffri.
Processen begynder med, at vedvarende energi udnyttes og omdannes til elektricitet. Denne elektricitet tilføres derefter til et elektrolyseanlæg, som bruger den til at spalte vandmolekyler i brint og ilt. Elektrolyse af vand effektivitet er afgørende for denne proces. Den resulterende grønne brint kan opbevares i tanke eller underjordiske lagre, indtil det er nødvendigt.
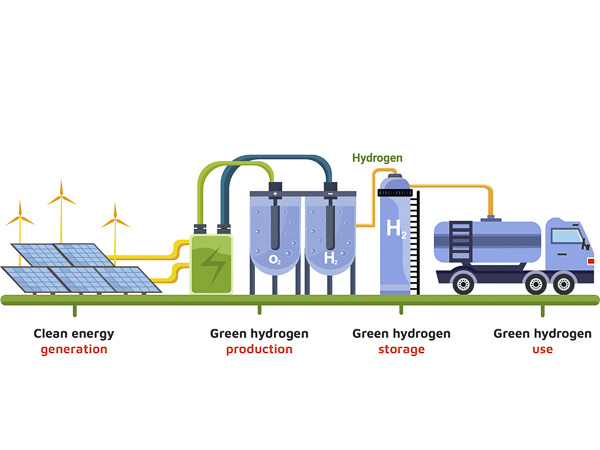
Når grøn brint er produceret, kan den transporteres gennem rørledninger eller via specialiserede transportkøretøjer til forskellige forbrugere, herunder industrier, tankstationer for brændselscellekøretøjer og endda kraftværker, der omdanner brint tilbage til elektricitet i perioder med høj efterspørgsel efter energi. Hvad skal en brændselscelle have tilført for at lave elektrisk energi? Svaret er brint, der bruges som brændstof i brændselsceller. Denne cyklus sikrer, at den energi, der genereres fra vedvarende kilder, ikke går til spilde og kan bruges, selv når solen ikke skinner eller vinden ikke blæser, hvilket giver en stabil og pålidelig energiforsyning.
Typer af elektrolyseanlæg
Der findes tre primære typer elektrolyseanlæg, som hver bruger forskellige teknologier og betingelser:
- Polymer Elektrolyt Membran (PEM) Elektrolyseanlæg: Disse elektrolyseanlæg bruger en solid polymembran som elektrolyt. De opererer ved relativt lave temperaturer (50-80°C) og tilbyder hurtige responstider, hvilket gør dem egnede til intermitterende vedvarende energikilder. PEM-elektrolyseanlæg er kompakte og modulære, men de har tendens til at være dyrere på grund af omkostningerne ved membranmaterialet.
- Alkaliske elektrolyseanlæg: Disse har været brugt i årtier og anvender en flydende alkalisk opløsning, normalt kaliumhydroxid, som elektrolyt. De opererer ved moderate temperaturer og er kendt for deres omkostningseffektivitet og lange kommercielle historie. De er dog generelt mindre effektive og langsommere til at reagere sammenlignet med PEM-elektrolyseanlæg.
- Solid Oxide Elektrolyseanlæg (SOEC): Disse opererer ved høje temperaturer (ca. 700-800°C) og bruger et fast keramisk materiale som elektrolyt. SOEC-elektrolyseanlæg tilbyder højere effektivitet ved at udnytte spildvarme fra industrielle processer eller koncentreret solenergi. De er særligt velegnede til storskala brintproduktion.
Hvilken elektrolysemetode er bedst?
Valget af den bedste elektrolysemetode afhænger af forskellige faktorer, herunder skalaen af brintproduktion, tilgængeligheden af varmekilder og integrationen med vedvarende energisystemer. PEM-elektrolyseanlæg er ideelle til applikationer, der kræver brint af høj renhed og hvor vedvarende energikilder er variable. Alkaliske elektrolyseanlæg er omkostningseffektive til industrielle applikationer med stabile energikilder. SOEC-elektrolyseanlæg er bedst til storskala operationer, hvor høje temperaturkilder er tilgængelige, hvilket giver højere effektivitet og bedre integration med industrielle processer.
Elektrolyse af vand effektivitet
Effektiviteten af et elektrolyseanlæg er en kritisk faktor i den samlede levedygtighed af brintproduktion. Det refererer til mængden af elektrisk energi, der kræves for at producere en bestemt mængde brint. SOEC-elektrolyseanlæg er typisk mere effektive med en effektivitet på 10-26% højere end PEM- og alkaliske elektrolyseanlæg på grund af deres evne til at operere ved højere temperaturer og udnytte spildvarme.
Elektrolyseanlæg og brændselscelle - En sammenligning
Det er vigtigt at forstå forskellen mellem et elektrolyseanlæg og en brændselscelle. Mens et elektrolyseanlæg bruger elektricitet til at producere brint, gør en brændselscelle det modsatte ved at omdanne brint til elektricitet gennem en kemisk reaktion med ilt, typisk til energiproduktion i køretøjer og stationære applikationer. Hvad skal en brændselscelle have tilført for at lave elektrisk energi? Svaret er, at den skal tilføres brint og ilt. Debatten om brændselscelle vs. elektrolyseanlæg drejer sig om deres roller i brintøkonomien: elektrolyseanlæg er til brintproduktion, mens brændselsceller er til brintudnyttelse.
Opsummering
Rollen af brintelektrolyseanlæg i det bæredygtige energilandskab kan ikke overvurderes. De giver en vej til produktion af grøn brint, som kan bidrage til at afkarbonisere forskellige industrier og tilbyde et nul-emissionsalternativ til transport. Efterhånden som teknologien udvikler sig og effektiviteten forbedres, vil elektrolyseanlæg spille en afgørende rolle i overgangen til en grønnere og mere bæredygtig fremtid.
Elektrolyseanlæg står i spidsen for denne brintrevolution, som forbinder vedvarende energikilder med praktiske anvendelser af ren energi i hverdagen. Fortsat forskning, innovation og investeringer på dette område lover at låse op for nye potentialer og drive den globale overgang mod en bæredygtig energifremtid.
Kilder: Topsoe.com, energy.gov og chemicals.co.uk

